Aminosäuren
Aminosäuren sind organische Verbindungen mit mindestens einer Carboxygruppe, einer Aminogruppe und einem organischen Rest. Aminosäuren sind die Bausteine der Proteine.
Themen auf dieser Seite
- Aminosäuren Struktur und Eigenschaften
- Aminosäuren als Zwitterionen
- Übersicht von Aminosäuren
- Elektrophorese
Neu!
Aminosäuren Struktur und Eigenschaften
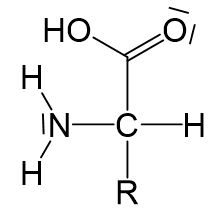
Ist die Aminogruppe an dem Kohlenstoffatom neben der Carboxygruppe (α-C-Atom) gebunden, so wird die Aminosäure als α-Aminosäure bezeichnet. Ist sie am nächsten Kohlenstoffatom gebunden, so handelt es sich um eine β-Aminosäure.
α-Aminosäuren haben ein Chiralitätszentrum am α-Kohlenstoffatom, weshalb die räumliche Anordnung der Substituenten wichtig ist. Es gibt also zu jedem Molekül eine D- und eine L-Form (Bild und Spiegelbild), wobei die Bezeichnung von der Position der Aminogruppe in der Fischerprojektion abhängt. Proteine höherer lebender Organismen sind Polymere aus hauptsächlich α-L-Aminosäure.
Aminosäuren als Zwitterionen
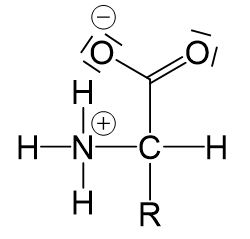
Aufgrund der Carboxygruppe sind Aminosäuren Protonendonatoren, und aufgrund der Aminogruppe gleichzeitig Protonenakzeptoren. Durch intramolekulare Protonenwanderung kann das Proton der Carboxygruppe abgegeben- und durch das freie Elektronenpaar der Aminogruppe aufgenommen werden. Das entstehende Molekül wird Zwitterion genannt.
Aminosäuren liegen als Feststoff und in wässrigen Lösungen überwiegend als Zwitterionen vor- also mit deprotonierter Carboxygruppe und protonierter Aminogruppe.
Aminosäuren sind Ampholyte, da die deprotonierte Carboxygruppe Protonen aufnehmen- und die protonierte Aminogruppe Protonen abgeben kann. In saurer Lösung reagieren sie demnach als Basen und liegen als Kation vor.
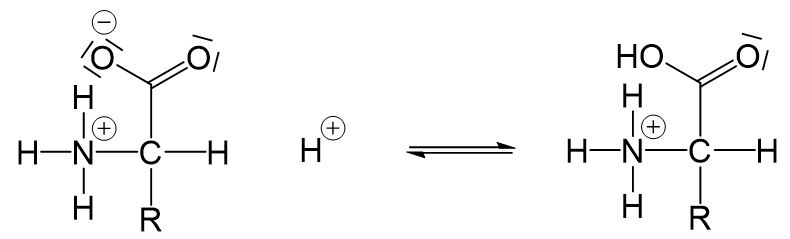
In basischen Lösungen reagieren sie als Säuren und liegen als Anion vor.
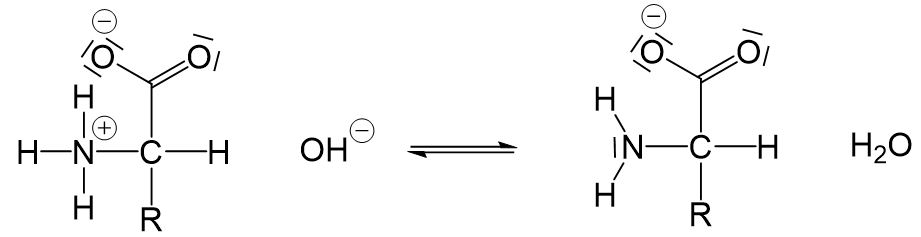
Je nach pH-Wert kann eine Aminosäure als Kation, Anion oder Zwitterion vorliegen. Der pH-Wert, bei dem sie nahezu ausschließlich als Zwitterion vorliegen, ist der sogenannte isoelektrische Punkt (IEP). Dieser ist, aufgrund der Effekte der organischen Reste, bei allen Aminosäuren unterschiedlich.
Aminosäuren Schmelztemperatur
Da Aminosäuren als Reinstoff als Zwitterionen vorliegen sind die zwischenmolekularen Wechselwirkungen sehr hoch, da es sich hier um Ionenbindungen (Anziehung zwischen positiver und negativer Ladung) handelt. Um diese Ionenbindungen zu überwinden wird sehr viel Energie benötigt. Meistens ist die benötigte Energie so hoch, dass Atombindungen aufgebrochen werden und das Aminosäuremolekül zerstört wird. Daher können die meisten Aminosäuren nicht geschmolzen werden.
Neu!
Löslichkeit von Aminosäuren
Aufgrund der positiven und der negativen Ladung im Zwitterion, weist das Molekül im Bereich des α-C-Atoms eine hohe Polarität auf. Daher sind die meisten Aminosäuren gut in polaren Lösungsmitteln wie Wasser löslich. Die Löslichkeit der Aminosäure in Wasser hängt jedoch auch von dem organischen Rest ab. Je größer und unpolarer dieser Rest wird, desto schlechter ist die Aminosäure in Wasser löslich.
Übersicht von Aminosäuren
Aminosäuren werden nicht mit IUPAC-Namen angegeben, sondern mit sognannten Trivialnamen. Diese muss man lernen. Von diesen Namen leiten sich die jeweiligen Abkürzungen, die oft verwendet werden, ab.
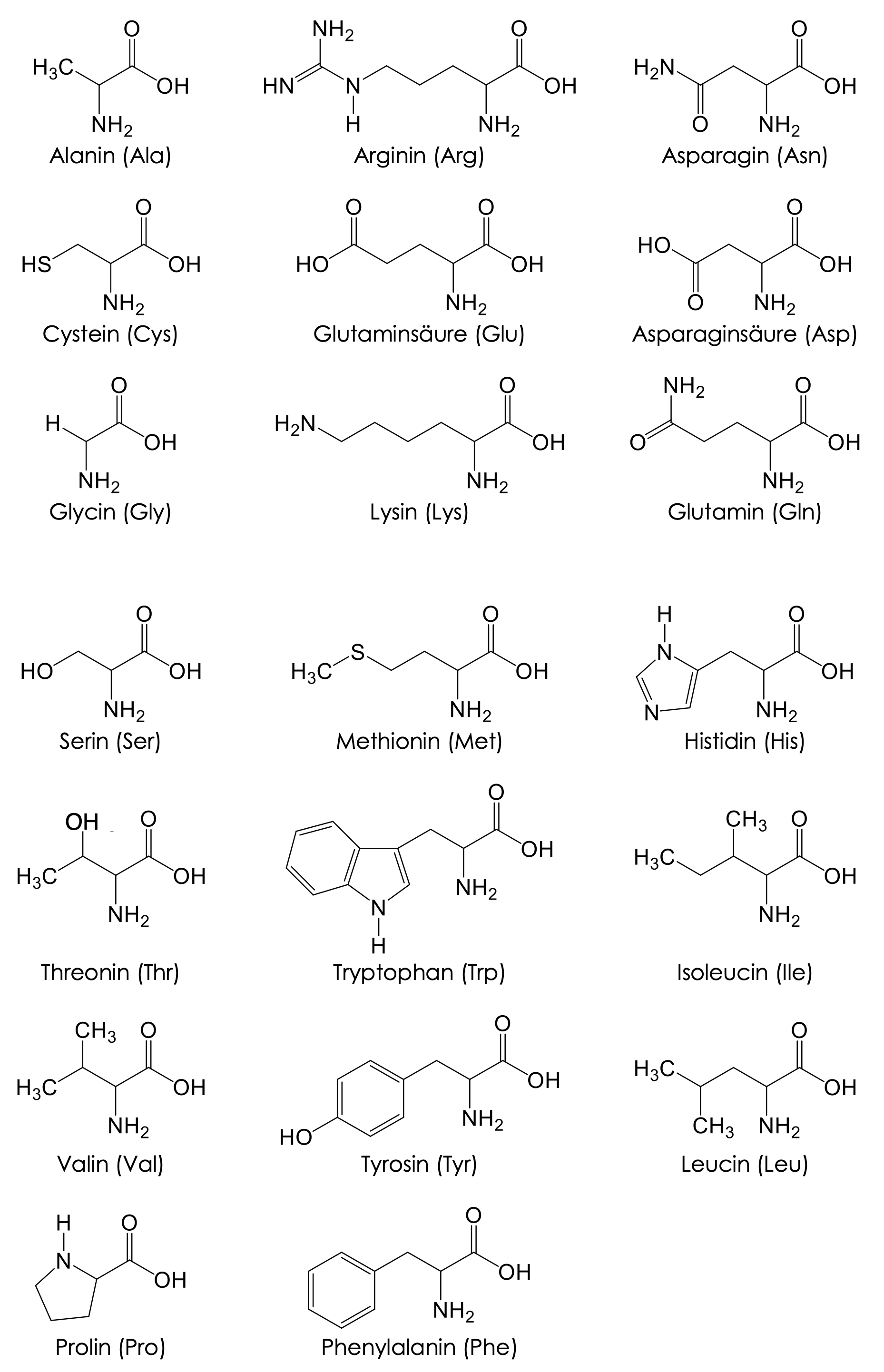
Elektrophorese
Die Elektrophorese ist eine Methode um Gemische aus Aminosäuren zu trennen. Dabei wird die Eigenschaft genutzt, dass die isoelektronischen Punkte der Aminosäuren verschieden sind und bei einem bestimmten pH-Wert manche Aminosäuren als Kationen, mache als Anionen und manche als Zwitterionen vorliegen.
Um das Gemisch zu trennen wird die Probe gelöst und ein bestimmter pH-Wert eingestellt. Man gibt ein paar Tropfen dieser Probe auf ein feuchtes Filterpapier, welche mit einem Plus- und einem Minuspol verbunden ist.
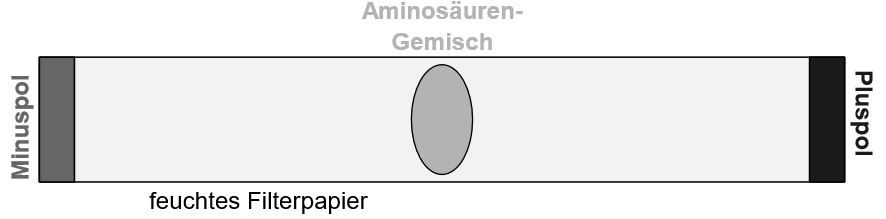
Positiv geladene Aminosäuren wandern zum negativ geladenen Minuspol, negativ geladenen Aminosäuren wandern zum positiv geladenen Pluspol. Haben die Aminosäuren einen großen Rest, dann sind sie schwerer und wandern daher langsamer als Aminosäuren mit kleinem Rest.
Zwitterionen wandern gar nicht, da sie nach außen nicht geladen sind. Nach einer gewissen Zeit sieht das Filterpapier dann folgendermaßen aus:
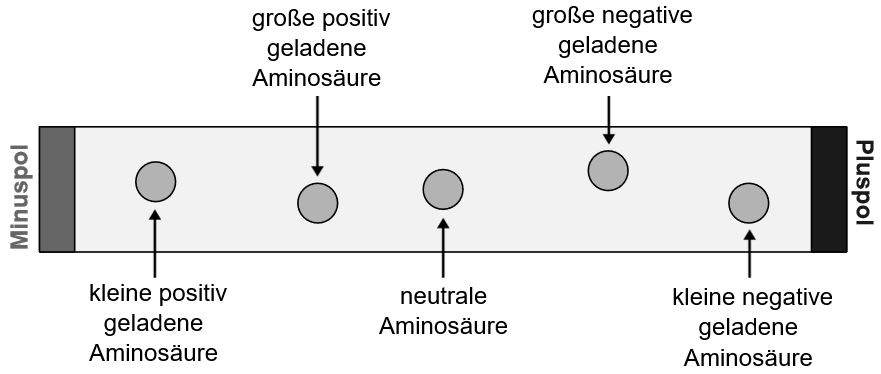
Neu!