Kohlenwasserstoffe
In der organischen Chemie bestehen Moleküle überwiegend aus den Elementen Kohlenstoff und Wasserstoff. Verbindungen, welche nur diese beiden Elemente enthalten, heißen Kohlenwasserstoffe. Die wichtigsten Grundlagen rund um das Thema Kohlenwasserstoffe erklären wir dir in diesem Artikel.
Neu!
Themen auf der Seite:
Wichtige Grundlage
Kohlenwasserstoffe können in gesättigte und ungesättigte Kohlenwasserstoffe aufgeteilt werden.
- Gesättigt bedeutet, dass alle Valenzen (freie Plätze zum Andocken) des Kohlenwasserstoffes besetzt sind. Somit ist die maximal mögliche Anzahl an Wasserstoffatomen in einem Molekül erreicht und es können keine weiteren Atome aufgenommen werden.
- Ungesättigte Kohlenwasserstoffe können Mehrfachbindungen (Alkene und Alkine) eingehen. Ihre Valenzen sind nicht vollständig besetzt. Hierdurch besteht die Möglichkeit, dass weitere sich weitere Atome mit dem Kohlenwasserstoff verbinden können
Alkane
Alkane sind, wie bereits oben beschrieben, gesättigte Kohlenwasserstoffe mit der allgemeinen Summenformel $C_n H_{2n+2}$. Der Name der Alkane ist abhängig von der Anzahl der Kohlenstoffatome.
In der folgenden Tabelle findest du eine Übersicht der wichtigsten Alkane. Diese Namen musst du unbedingt auswendig lernen, da diese die Grundlage für alle Molekülnamen bilden.
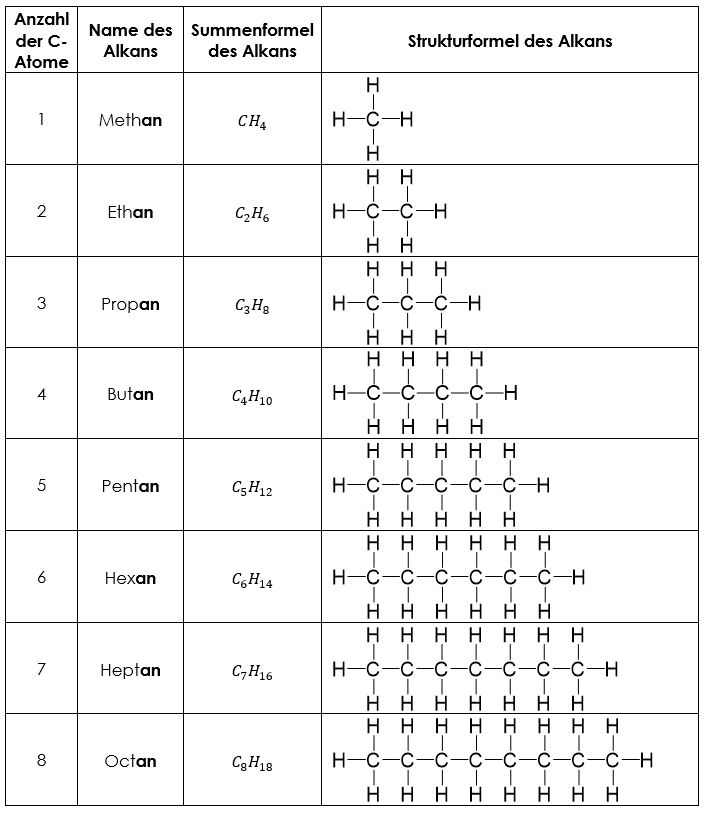
Die Alkane in der Tabelle sind unverzweigt. Dies bedeutet, dass maximal zwei Kohlenstoffatome an ein anderes Kohlenstoffatom gebunden sind. Die Möglichkeit, dass Alkane verzweigt sind, besteht dennoch.
Neu!
Alkene
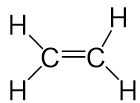
Alkene sind ungesättigte Kohlenwasserstoffe, die Doppelbindungen enthalten. Durch diese Doppelbindungen sind weniger Wasserstoffatome im Molekül gebunden als bei Alkane. Die allgemeine Summenformel lautet: $C_n H_2n$.
Der Name der Alkene und somit ihre Wortendungen „-en“ leiten sich von der Anzahl der Kohlenstoffatome und somit vom entsprechenden Alkan ab. Es handelt sich bei dem Alken mit zwei Kohlenstoffatomen also um Ethen.
Alkine
Alkine sind ebenfalls ungesättigte Kohlenwasserstoffe, die im Gegensatz zu den Alkenen jedoch keine Doppelbindungen, sondern Dreifachbindungen- und entsprechend noch weniger Wasserstoffatome enthalten. Die allgemeine Summenformel lautet $C_n H_(2n-2)$. Auch hier leitet sich der Name von der Anzahl der Kohlenstoffatome- und somit von dem entsprechenden Alkan ab, indem man statt der Endung -an die Endung -in verwendet. Bei einem Alkin mit zwei Kohlenstoffatomen handelt es sich also um Ethin.
![]()
Schmelz- und Siedepunkte von Kohlenwasserstoffen
Oft soll man zwei Moleküle bezüglich ihrer Schmelz- und Siedepunkte vergleichen, also angeben, bei welchem Molekül diese höher sind. Beim Schmelzen oder Sieden eines Stoffes werden die zwischenmolekularen Wechselwirkungen überwunden.
Je niedriger die zwischenmolekularen Wechselwirkungen sind, desto weniger Energie wird benötigt, um einen Stoff zu schmelzen oder zu sieden. Der Schmelz- bzw. Siedepunkt liegt demnach niedriger.
Um den Schmelz- bzw. Siedepunkt eines Stoffs einschätzen zu können, muss man also wissen, welche Art von zwischenmolekularen Wechselwirkungen vorliegen und wie stark diese sind.
[/box-info]-
- Bei Kohlenwasserstoffen sind die einzigen zwischenmolekularen Wechselwirkungen, die vorliegen, die van-der-Waals-Wechselwirkungen. Diese lassen sich nach folgenden Kriterien einschätzen:
- Je länger die Kette der Kohlenwasserstoffe, desto stärker sind die van-der-Waals-Kräfte.
- Je verzweigter das Molekül ist, desto schwächer sind die van-der-Waals-Kräfte.
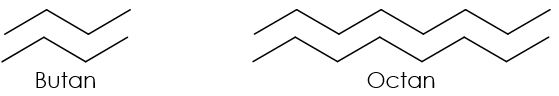
Bei den Butanmolekülen ist die Fläche, an der die van-der-Waals-Kräfte wirken können, kleiner als bei den Octanmolekülen. Daher sind diese Wechselwirkungen bei Octan höher als bei Butan. Das kannst du dir vorstellen wie bei einem Klebestreifen. Je länger der Klebestreifen ist, desto schwerer ist es ihn von der Oberfläche, auf der er klebt, herunterzuziehen.
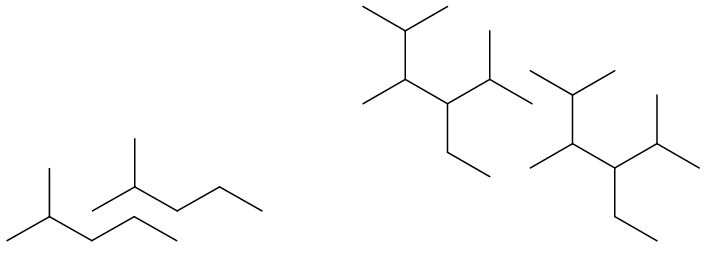
Bei den verzweigten Molekülen gilt dasselbe Prinzip: je besser man die Moleküle ineinander stapeln kann und somit die Oberfläche, an der die van-der-Waals-Kräfte wirken können, größer ist, desto stärker sind diese Wechselwirkungen. Je verzweigter ein Molekül ist, desto schlechter kann ich sie aneinander anlagern.
Löslichkeit von Kohlenwasserstoffen
Möchte man entscheiden, ob sich ein Stoff in einem anderen löst, muss man wissen, ob die Stoffe polar oder unpolar sind (genaueres dazu kannst du nachlesen in AC). Wenn man das weiß, muss man noch folgendes wissen:
Ähnliches löst sich in Ähnlichem, was bedeutet, dass sich polare Stoffe nur in polaren lösen und unpolare nur in unpolaren.
Da Kohlenwasserstoffe nur unpolare Bindungen haben, sind auch die Moleküle unpolar. Sie können also nur in unpolaren Stoffen gelöst werden. Da Wasser ein polarer Stoff ist, können Kohlenwasserstoffe also nicht in Wasser gelöst werden.
Neu!
Löslichkeit von Kohlenwasserstoffen
In diesem Kapitel werden die typischen Reaktionen der Kohlenwasserstoffe aufgelistet.
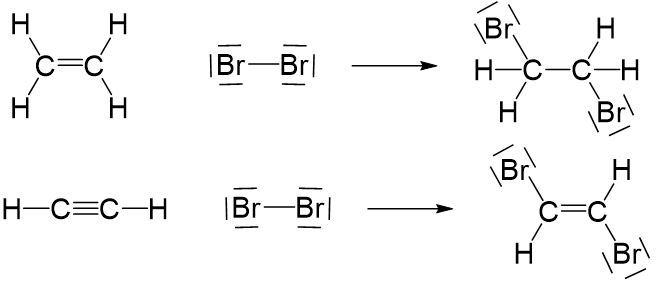
Alkane reagieren typischerweise unter einer sogenannten radikalischen Substitution mit Halogenen.
Alkene und Alkine reagieren typischerweise unter einer sogenannten elektrophilen Addition, wobei eine Mehrfachbindung aufgelöst wird.