Enzyme
Enzyme sind Proteine, die als Katalysatoren wirken. Enzyme beschleunigen die Reaktionsgeschwindigkeit von chemischen Reaktionen und regulieren Stoffwechselprozesse.
Als Katalysatoren setzen sie die Aktivierungsenergie von chemischen Reaktionen herab und werden selbst nicht verbraucht.
Zur Einführung in das Thema Enzyma kannst du dir jetzt das passende Lernvideo anschauen!
Wirkungsweise von Enzymen
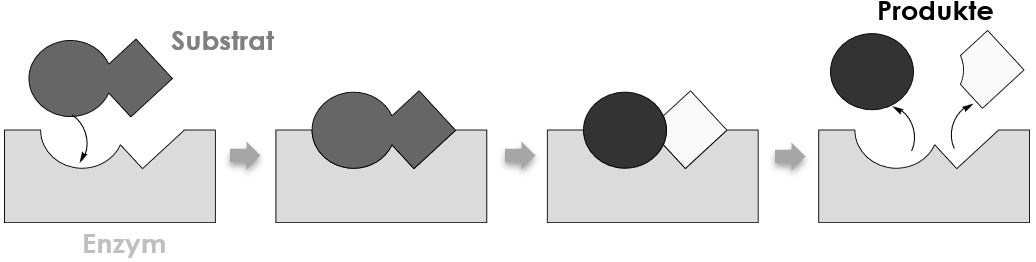
Damit Enzyme ihre Funktion ausführen können, wird der umzusetzende Stoff (Substrat) an eine bestimmte Stelle des Enzyms, das sogenannte aktive Zentrum, über zwischenmolekulare Wechselwirkungen gebunden. Es entsteht ein Enzym-Substrat-Komplex. Das Substrat wird nun umgesetzt und anschließend das Reaktionsprodukt wieder von dem Enzym gelöst. Das Enzym steht dadurch für neue Substratumsetzungen zu Verfügung.
Enzym Schlüssel-Schlossprinzip
Enzyme können allerdings nicht jedes beliebige Substrat umsetzen. Die Tertiärstruktur spielt dabei eine große Rolle. Durch die Tertiärstruktur hat das Enzym eine Einbuchtung, in die das Substrat reinpasst. Dabei wirken Enzym und Substrat nach dem Schlüssel-Schloss-Prinzip. Passt das Substrat nicht in die Einbuchtung des Enzyms, so kann es auch nicht darin gebunden und umgesetzt werden.
Substratspezifität von Enzymen
Enzyme können also nur bestimmte Substrate umsetzen. Diese Eigenschaft nennt man Substratspezifität. Dabei unterscheidet man die Gruppenspezifität und die absolute Spezifität. Enzyme mit einer absoluten Spezifität können nur ein bestimmtes Substrat umsetzen, Enzyme mit einer Gruppenspezifität können Substrate mit gleichen funktionellen Gruppen umsetzen. Die Alkoholhydrogenase setzt beispielsweise Alkohole wie Ethanol und Methanol in die entsprechenden Aldehyde Ethanal und Methanal um.
Neu!
Wirkungsspezifität von Enzymen
Enzyme sind nicht nur substratspezifisch, sondern auch wirkungsspezifisch. Das bedeutet, dass ein Substrat welches an ein Enzym gebunden ist nur auf eine ganz bestimmte Weise umgesetzt werden kann. Ein anderes Enzym kann das Substrat auf eine andere Weise umsetzen.
Enzymaktivität
Die Enzymaktivität beschreibt, wie viele Substratmoleküle ein Enzym pro Minute umsetzt. Diese ist abhängig von verschiedenen Faktoren wie Substratkonzentration, Temperatur und pH-Wert.
Passend zur Enzymaktivität hat unser Partner Die Merkhilfe ein Lernvideo erstellt! Schau es dir jetzt an!
Substratkonzentration
Die Enzymaktivität hängt von er Substratkonzentration ab.
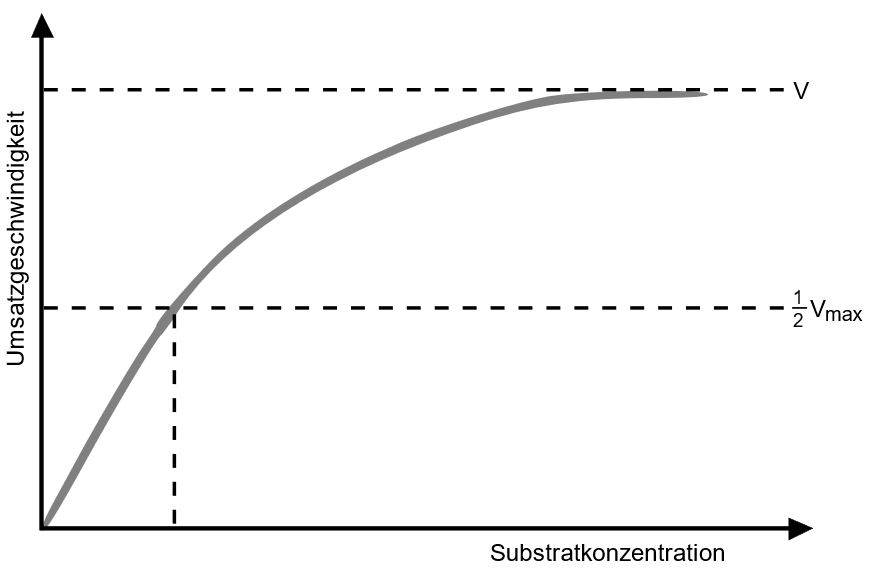
Mit steigender Substratkonzentration steigt die Umsatzgeschwindigkeit. Das liegt daran, dass genügend Enzymmoleküle vorhanden sind, um jedes Substratmolekül umzusetzen. Daher steigt die Umsatzgeschwindigkeit zunächst proportional zur Substratkonzentration.
Werden noch mehr Substratmoleküle hinzugegeben steigt die Umsatzgeschwindigkeit zwar weiter, aber nicht mehr so schnell wie bisher, da die freien Enzymmoleküle nun immer seltener werden. Daher dauert es länger, bis die Substratmoleküle und die freien Enzymmoleküle aufeinandertreffen.
Irgendwann ist der Punkt erreicht, an dem alle Enzymmoleküle besetzt sind und eine weitere Erhöhung der Umsatzgeschwindigkeit nicht mehr möglich ist. Es gibt also eine maximale Umsatzgeschwindigkeit.
Neu!
Auswirkung der Temperatur auf Enzymaktivität
Die Enzymaktivität ist auch abhängig von der Temperatur. Zunächst bewirkt eine Temperaturerhöhung auch eine Erhöhung der Umsatzgeschwindigkeit (Prinzip der RGT-Funktion). Das liegt daran, dass sich die Teilchen bei einer höheren Temperatur schneller bewegen und sie somit schneller aufeinandertreffen.
Erhöht man die Temperatur aber weiter, so kommt es irgendwann zu einer sogenannten Hitzedenaturierung, das heißt die Tertiärstruktur der Enzyme wird verändert und sie können ihre Funktion nicht weiter ausüben.
Daher gibt es ein Temperaturoptimum, bei dem die Temperatur hoch genug ist, damit die Teilchen sich schnell bewegen, aber noch nicht so hoch, dass die Denaturierung eintritt.
Der Einfluss vom pH-Wert auf die Enzymaktivität
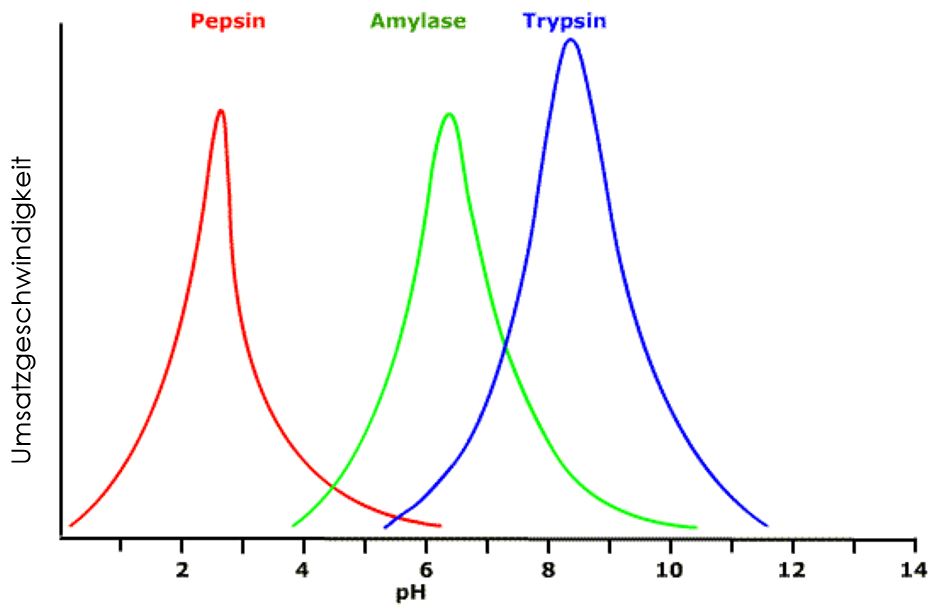
Ein weiterer Einflussfaktor für die Enzymaktivität ist der pH-Wert. Für jedes Enzym gibt es einen pH-Wert, bei dem es am aktivsten ist. Dieser pH-Wert ist das pH-Optimum eines Enzyms. Das liegt daran, dass Proteine verschiedene Gruppen enthalten, die bei pH-Wert-Änderungen protoniert oder deprotoniert werden. Dadurch können zwischenmolekulare Wechselwirkungen wegfallen oder zusätzliche entstehen, was dazu führt, dass sich die Tertiärstruktur verändert.
Einfluss von Hemmstoffen auf Enzymaktivität
Hemmstoffe sind Substanzen, welche die Enzymaktivität verringern und somit die Wirkungsweise von Enzymen hemmen. Es gibt verschiedene Hemmstoffe mit unterschiedlichen Wirkungsweisen.
Im folgenden Lernvideo wird dir erklärt, wie Enzyme gehemmt werden!
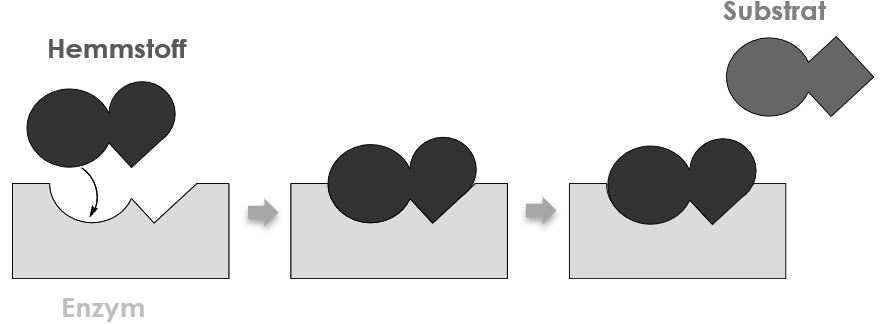
Kompetitive Hemmung
Hemmstoffe, welche eine kompetitive Hemmung verursachen haben eine ähnliche Struktur wie das Substrat. Dadurch kann es am aktiven Zentrum des Enzyms reversibel gebunden werden und es entsteht ein Enzym-Hemmstoff-Komplex. Im Gegensatz zum Substrat kann der Hemmstoff durch das Enzym aber nicht umgesetzt werden und blockiert das Enzym.
Diese Art von Hemmung kann durch die Erhöhung der Substratkonzentration aufgehoben werden.
Nichtkompetitive Hemmung
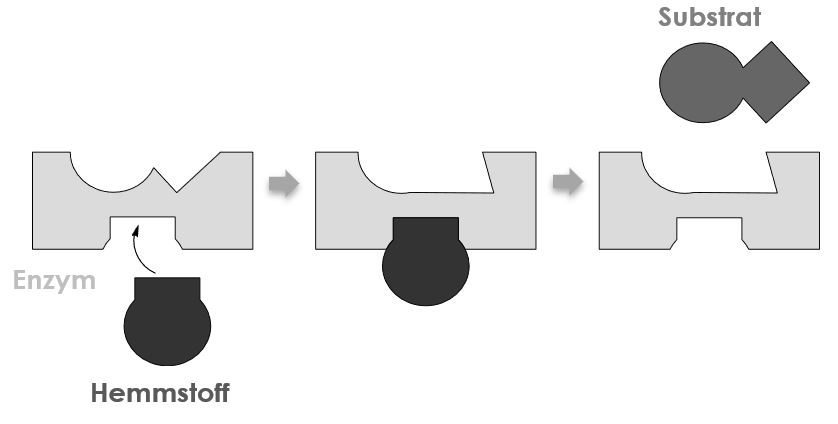
Hemmstoffe, welche eine nichtkompetitive Hemmung verursachen haben keine Ähnlichkeit mit dem Substrat. Sie werden daher nicht am aktiven Zentrum, sondern an einer anderen Stelle des Enzyms reversibel gebunden. Diese Stelle wird allosterisches Zentrum genannt. Durch die Bindung am allosterischen Zentrum wird die räumliche Struktur des Enzyms verändert, wodurch das Substrat nicht mehr am aktiven Zentrum gebunden werden kann.
Diese Art der Hemmung kann im Gegensatz zur kompetitiven Hemmung nicht durch die Erhöhung der Substratkonzentration aufgehoben werden.
Hemmung durch Schwermetallionen
Die Enzymaktivität kann auch durch Schwermetallionen (Quecksilber-, Blei-, Kupferionen, …) gehemmt werden. Die Schwermetallionen können irreversibel an die Seitengruppen (Amino-, Sulfid-, Carboxygruppe, …) gebunden werden. Dadurch werden die zwischenmolekularen Wechselwirkungen und somit auch die Tertiärstruktur verändert, wodurch das Substrat nicht mehr am Enzym gebunden werden kann.
Neu!